
Стабильный pH — это основа эффективного питания растений. Если кислотность раствора выходит за пределы оптимальных значений, одни элементы становятся недоступными, а другие — токсичными. При этом большинство методов коррекции pH — это борьба с последствиями: сегодня добавили кислоту, завтра щёлочь, послезавтра опять кислоту. Такая «качель» не только неудобна, но и может навредить корням.
Simplex pH Perfect — это не просто регулятор кислотности. Это буферный комплекс, созданный для того, чтобы раствор сам стремился к стабильному значению pH около 6,0–6,1 +/-0,3 — даже если вы добавляете удобрения, воду разного качества или микроэлементы. Он не понижает и не повышает pH «на глаз», а удерживает его в нужной зоне, за счёт чётко рассчитанного химического механизма.
Чтобы понять, как это работает, придётся немного вспомнить школьную химию. Без этого не обойтись, поскольку pH Perfect не просто меняет кислотность, а именно стабилизирует её в оптимальном диапазоне значений.
Чтобы понять, как это работает, придётся немного вспомнить школьную химию. Без этого не обойтись, поскольку pH Perfect не просто меняет кислотность, а именно стабилизирует её в оптимальном диапазоне значений.
Что такое pH и почему он важен
Чтобы понять принцип работы pH Perfect, начнём с понятия диссоциации. Это процесс, при котором нейтральные молекулы распадаются на заряженные частицы — ионы.
Пример диссоциации соляной кислоты (HCl):
HCl ⇌ H⁺ + Cl⁻
Такая реакция обратима, и не все молекулы распадаются полностью — но нам сейчас важно другое: ион водорода (H⁺), он же протон, и есть источник кислотности. Чем больше таких протонов в растворе, тем более кислым он становится.
А вот основания, наоборот, дают гидроксид-ион (OH⁻). Например:
KOH ⇌ K⁺ + OH⁻
Количество ионов OH⁻, растворенных в воде, определяет её уровень щелочности. Чем больше их в растворе, тем более щелочным он становится.
Получается, всё сводится к количеству H⁺ и OH⁻ в растворе. В нейтральной воде их одинаковое количество — примерно 10⁻⁷ моль на литр каждого. Именно отсюда берётся привычное значение pH = 7.
pH среды/раствора — это концентрация содержащихся в ней протонов.
Этот показатель считается по логарифмической формуле:
pH = –log[H⁺]
То есть если концентрация протонов равна 10⁻⁷, логарифм от 10⁻⁷ равен –7, а pH — это просто 7. Вот почему шкала pH логарифмическая: каждое целое значение — это 10-кратная разница в кислотности.
Это действительно важно для понимания того, почему даже небольшие колебания pH могут очень сильно влиять на состояние растений. Если pH будет равен 5, то среда будет уже в 100 раз кислее, чем при pH = 7.
Можно ввести и обратную величину — pOH, связанную с концентрацией OH⁻. Сумма двух значений всегда даёт 14:
pH + pOH = 14
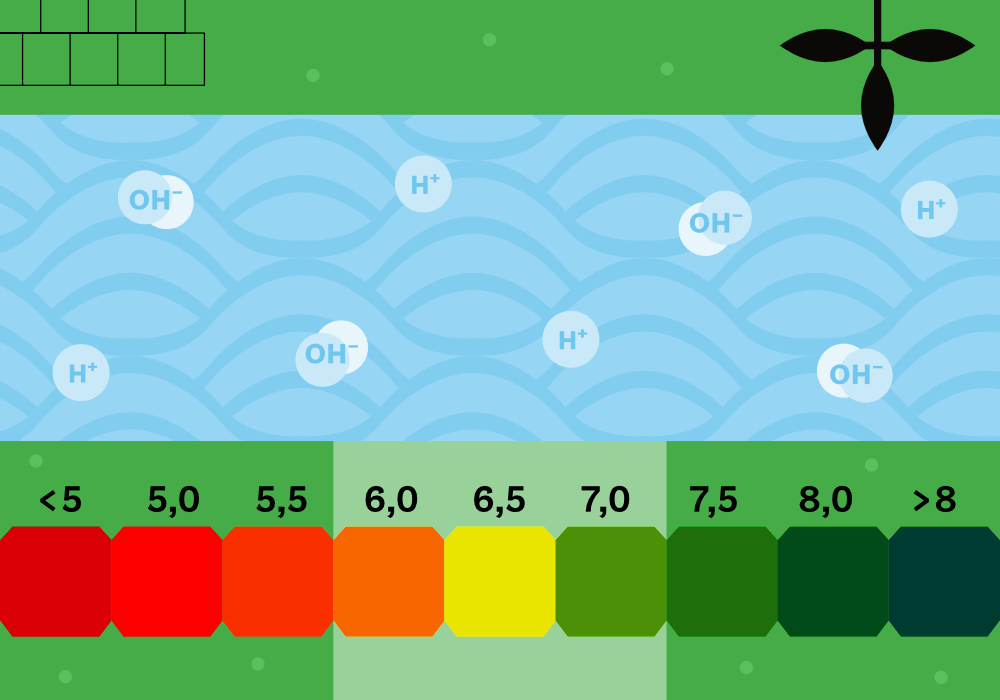
Это и формирует привычную шкалу от 0 до 14:
Для большинства культивируемых растений оптимальной считается слабокислая среда (5,5–6,5 pH). В более кислой или щелочной среде значительно снижается эффективность усвоения корнями питательных элементов. Крайние значения могут даже полностью загубить растение.
Пример диссоциации соляной кислоты (HCl):
HCl ⇌ H⁺ + Cl⁻
Такая реакция обратима, и не все молекулы распадаются полностью — но нам сейчас важно другое: ион водорода (H⁺), он же протон, и есть источник кислотности. Чем больше таких протонов в растворе, тем более кислым он становится.
А вот основания, наоборот, дают гидроксид-ион (OH⁻). Например:
KOH ⇌ K⁺ + OH⁻
Количество ионов OH⁻, растворенных в воде, определяет её уровень щелочности. Чем больше их в растворе, тем более щелочным он становится.
Получается, всё сводится к количеству H⁺ и OH⁻ в растворе. В нейтральной воде их одинаковое количество — примерно 10⁻⁷ моль на литр каждого. Именно отсюда берётся привычное значение pH = 7.
pH среды/раствора — это концентрация содержащихся в ней протонов.
Этот показатель считается по логарифмической формуле:
pH = –log[H⁺]
То есть если концентрация протонов равна 10⁻⁷, логарифм от 10⁻⁷ равен –7, а pH — это просто 7. Вот почему шкала pH логарифмическая: каждое целое значение — это 10-кратная разница в кислотности.
Это действительно важно для понимания того, почему даже небольшие колебания pH могут очень сильно влиять на состояние растений. Если pH будет равен 5, то среда будет уже в 100 раз кислее, чем при pH = 7.
Можно ввести и обратную величину — pOH, связанную с концентрацией OH⁻. Сумма двух значений всегда даёт 14:
pH + pOH = 14
Это и формирует привычную шкалу от 0 до 14:
- pH = 0 — максимум H⁺, кислота
- pH = 7 — равновесие
- pH = 14 — максимум OH⁻, щёлочь
Для большинства культивируемых растений оптимальной считается слабокислая среда (5,5–6,5 pH). В более кислой или щелочной среде значительно снижается эффективность усвоения корнями питательных элементов. Крайние значения могут даже полностью загубить растение.
На этом уровне уже можно понять, почему pH так важен. Но чтобы понять, как именно его стабилизирует pH Perfect, нужно взглянуть на механизм взаимодействия кислот и оснований.
Как взаимодействуют кислоты и основания
Когда кислота встречается с основанием, между ними происходит реакция нейтрализации. И, несмотря на всё химическое разнообразие, суть у этой реакции всегда одна и та же: протон (H⁺) встречается с гидроксид-анионом (OH⁻) и образует воду.
Рассмотрим пример: соляная кислота (HCl) и гидроксид калия (KOH).
Молекулярное уравнение:
HCl + KOH → KCl + H₂O
Если записать это в ионной форме (учитывая, что оба вещества полностью диссоциируют в растворе), получим:
H⁺ + Cl⁻ + K⁺ + OH⁻ → K⁺ + Cl⁻ + H₂O
Ион калия (K⁺) и хлорид-ион (Cl⁻) с обеих сторон уравнения не изменились — значит, они зрители, не участвующие в сути процесса. Уберём их и получим сокращённое ионное уравнение:
H⁺ + OH⁻ → H₂O
Это и есть основа: любая кислота и любое основание реагируют именно так. Их «хвосты» (анионы и катионы) потом образуют соль, но pH определяет только то, сколько протонов и гидроксид-ионов есть в растворе.
Рассмотрим пример: соляная кислота (HCl) и гидроксид калия (KOH).
Молекулярное уравнение:
HCl + KOH → KCl + H₂O
Если записать это в ионной форме (учитывая, что оба вещества полностью диссоциируют в растворе), получим:
H⁺ + Cl⁻ + K⁺ + OH⁻ → K⁺ + Cl⁻ + H₂O
Ион калия (K⁺) и хлорид-ион (Cl⁻) с обеих сторон уравнения не изменились — значит, они зрители, не участвующие в сути процесса. Уберём их и получим сокращённое ионное уравнение:
H⁺ + OH⁻ → H₂O
Это и есть основа: любая кислота и любое основание реагируют именно так. Их «хвосты» (анионы и катионы) потом образуют соль, но pH определяет только то, сколько протонов и гидроксид-ионов есть в растворе.
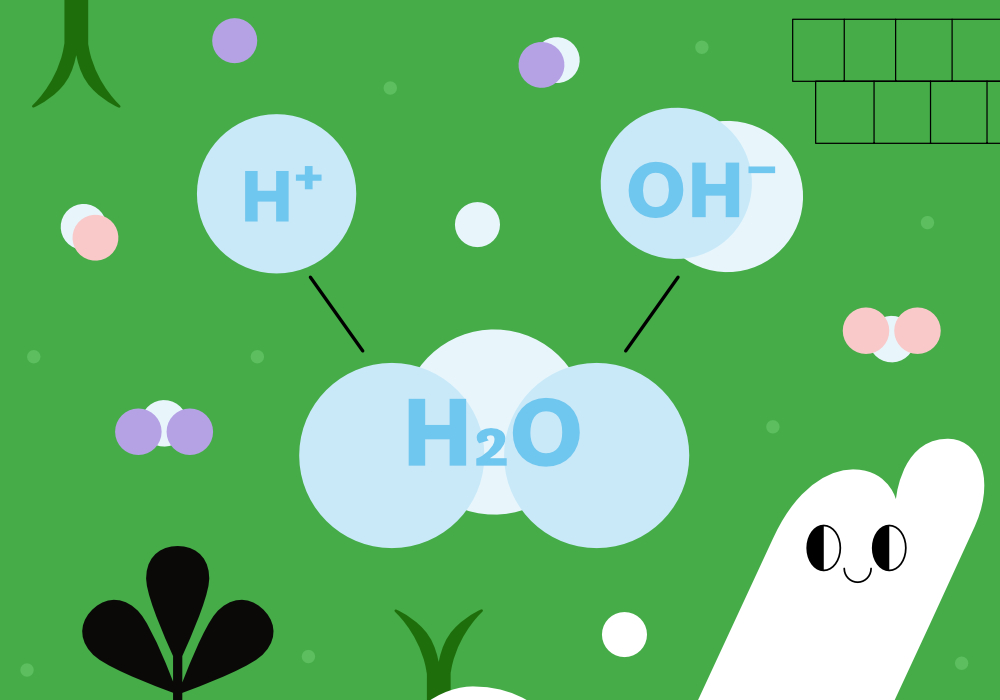
Вот почему регулирование pH — это всегда работа с этими двумя частицами. А теперь представим, что вместо того, чтобы вручную добавлять кислоту или щёлочь, в растворе будет система, способная сама улавливать лишние H⁺ или OH⁻ и нейтрализовать их. Именно так и работает буфер — а значит и pH Perfect.
Как органические кислоты стабилизируют pH
В отличие от минеральных кислот, которые мы уже обсудили, органические кислоты действуют тоньше. Их сила не в агрессивности, а в структуре. А именно — в функциональных группах, которые определяют поведение молекулы в растворе.
Самая важная для нас группа — карбоксильная (–COOH). Именно она отвечает за кислотные свойства большинства органических соединений. В растворе она может диссоциировать, отдавая протон (H⁺) и превращаясь в карбоксилат-ион (–COO⁻).
Это делает такие кислоты слабыми, но именно благодаря этому они умеют делать то, что невозможно с более сильными кислотами: стабилизировать pH.
Некоторые органические кислоты содержат две и более карбоксильных группы — это так называемые многоосновные кислоты. Они не только более «кислотны», но и обладают двумя важными способностями:
Самая важная для нас группа — карбоксильная (–COOH). Именно она отвечает за кислотные свойства большинства органических соединений. В растворе она может диссоциировать, отдавая протон (H⁺) и превращаясь в карбоксилат-ион (–COO⁻).
Это делает такие кислоты слабыми, но именно благодаря этому они умеют делать то, что невозможно с более сильными кислотами: стабилизировать pH.
Некоторые органические кислоты содержат две и более карбоксильных группы — это так называемые многоосновные кислоты. Они не только более «кислотны», но и обладают двумя важными способностями:
- формировать буферные системы;
- образовывать хелаты с ионами металлов.
Буферные смеси: как это работает
Если в растворе смешать слабую кислоту и её соль (например, малоновую кислоту и её калиевую соль), то будет установлено равновесие. При добавлении новой кислоты (например, HCl), соль будет её нейтрализовывать, захватывая лишние протоны и превращаясь обратно в молекулу кислоты. А при добавлении щёлочи — наоборот, кислота свяжет OH⁻, превращаясь в соль.
Все эти процессы идут параллельно и постоянно, удерживая уровень кислотности в пределах определённого диапазона. Это и есть pH буфер.
Каждая такая буферная система имеет свой рК (pKa) — значение pH, к которому она стремится. В случае pH Perfect эта точка равновесия лежит в районе 6,0–6,1 +/-0,3 — именно то, что нужно для большинства культур и для хорошей доступности микроэлементов.
Буферные растворы также можно представить как «губку» для кислот и щелочей: они впитывают избыток ионов H⁺ или OH⁻ и удерживают pH на одном уровне, как губка удерживает влагу.
Все эти процессы идут параллельно и постоянно, удерживая уровень кислотности в пределах определённого диапазона. Это и есть pH буфер.
Каждая такая буферная система имеет свой рК (pKa) — значение pH, к которому она стремится. В случае pH Perfect эта точка равновесия лежит в районе 6,0–6,1 +/-0,3 — именно то, что нужно для большинства культур и для хорошей доступности микроэлементов.
Буферные растворы также можно представить как «губку» для кислот и щелочей: они впитывают избыток ионов H⁺ или OH⁻ и удерживают pH на одном уровне, как губка удерживает влагу.
Хелатирование: помощь при нестабильном pH
Ещё одна особенность многоосновных органических кислот — способность обволакивать ионы металлов и удерживать их в растворимой активной форме. Например, малоновая кислота может создать с магнием прочный и стабильный хелат. Даже если pH чуть «съехал», хелатированный элемент останется доступным для растения.
В отличие от обычных солей, которые легко выпадают в осадок при сдвиге pH, хелаты остаются растворимыми: ион металла оказывается «упакован» в органическую молекулу и не так чувствителен к изменениям среды. По аналогии с тем, как защитный костюм уберегает человека от агрессивных внешних условий, хелатная оболочка сохраняет активность элементов.
Вот на этих двух свойствах — буферность и хелатирование — основана работа pH Perfect. А теперь разберёмся, из чего он состоит и почему его компоненты делают препарат таким «умным».
В отличие от обычных солей, которые легко выпадают в осадок при сдвиге pH, хелаты остаются растворимыми: ион металла оказывается «упакован» в органическую молекулу и не так чувствителен к изменениям среды. По аналогии с тем, как защитный костюм уберегает человека от агрессивных внешних условий, хелатная оболочка сохраняет активность элементов.
Вот на этих двух свойствах — буферность и хелатирование — основана работа pH Perfect. А теперь разберёмся, из чего он состоит и почему его компоненты делают препарат таким «умным».
Почему pH Perfect работает: состав, поведение, результат
Секрет pH Perfect — в его точно подобранном составе. Это смесь многоосновных органических кислот и их солей, сбалансированная таким образом, чтобы раствор стремился к значению pH ≈ 6,0–6,1 +/-0,3. Именно в этом диапазоне растениям доступны практически все макро- и микроэлементы.
Компоненты продукта — ксенобиотики, то есть соединения, которые не усваиваются ни растениями, ни почвенной биотой. Это позволяет раствору долго сохранять стабильность: никто из живых организмов не «съест» эти вещества, нарушая баланс.
Компоненты продукта — ксенобиотики, то есть соединения, которые не усваиваются ни растениями, ни почвенной биотой. Это позволяет раствору долго сохранять стабильность: никто из живых организмов не «съест» эти вещества, нарушая баланс.
Как продукт действует в растворе
- Буферизует pH. Система кислота–соль улавливает лишние H⁺ или OH⁻, постоянно возвращая уровень pH к своей точке равновесия.
- Образует хелаты. В этой форме микроэлементы, особенно нестабильные (например, Fe, Mn, Mg), сохраняются в доступном виде даже при небольших колебаниях pH.
- Минимально влияет на EC. Органические кислоты — слабые электролиты, они почти не диссоциируют и слабо влияют на электропроводность раствора. Но так как в составе есть калиевая соль, pH Perfect слегка увеличивает содержание калия (K⁺) и может немного повысить EC.

Практическая польза pH Perfect
- Предотвращение резких колебаний pH при добавлении удобрений или смене воды.
- Защита микроэлементов от потери доступности и активности.
- Поддержание стабильности питания, что особенно важно в автоматизированных системах.
- Обеспечение предсказуемого уровня pH без необходимости ежедневной корректировки.
- Снижение стресса корневой системы при переходе между удобрениями или смене воды
Всё это делает буферный регулятор pH надёжным инструментом для тех, кто хочет не просто «поправить кислотность», а создать сбалансированную и устойчивую питательную среду для растений. При этом pH Perfect сочетается с любыми типами удобрений и не требует дополнительных корректировок при переходе на другие нутриенты.
Как применять pH Perfect
Этот продукт прост в использовании. Таблица сочетаемости для использования pH Perfect не требуется. Он не вступает в нежелательные реакции ни с какими удобрениями. Необходимо лишь соблюдать несколько важных рекомендаций по правильной дозировке и очередности действий.
Первичная настройка:
При первом запуске системы с pH Perfect (особенно в гидропонике), важно настроить буфер правильно:
Базовая схема применения:
Мониторинг и стабильность:
Первичная настройка:
При первом запуске системы с pH Perfect (особенно в гидропонике), важно настроить буфер правильно:
- Используйте стартовую дозу 5–7 мл на 1 л раствора.
- Измерьте pH через 15–30 минут. Если значение отличается от целевого диапазона (pH 6,0–6,1 +/-0,3), вносите pH Perfect малыми порциями (по 1–2 мл/л) до достижения цели.
- После первой настройки система войдёт в режим автоподдержки, и в дальнейшем дозировку можно уменьшить.
Базовая схема применения:
- Добавлять в готовый питательный раствор, после всех удобрений.
- Рекомендуемая дозировка — 2–4 мл на 1 л раствора, в зависимости от стабильности воды и количества добавленных компонентов.
Мониторинг и стабильность:
- В большинстве случаев необходимость в частом измерении pH отпадает уже после первой недели.
- Период стабилизации может составлять от 3 до 10 дней в зависимости от конкретных особенностей воды, состава раствора, температуры и культуры.

Важные рекомендации:
Благодаря буферным свойствам состава, pH Perfect не требует постоянного внесения — после первоначальной настройки раствор сам поддерживает нужное значение pH. При стандартных дозировках расход остаётся очень умеренным: одной упаковки хватает на длительное время даже при регулярном использовании. Это делает продукт не только удобным, но и экономически выгодным решением как для домашних гроверов, так и для профессионалов.
- Не смешивайте pH Perfect с другими компонентами до добавления в воду.
- Не превышайте рекомендуемые дозировки.
- Храните в прохладном, тёмном месте, вдали от детей.
Благодаря буферным свойствам состава, pH Perfect не требует постоянного внесения — после первоначальной настройки раствор сам поддерживает нужное значение pH. При стандартных дозировках расход остаётся очень умеренным: одной упаковки хватает на длительное время даже при регулярном использовании. Это делает продукт не только удобным, но и экономически выгодным решением как для домашних гроверов, так и для профессионалов.
pH Perfect — это не просто ещё один регулятор кислотности. Это продуманный с химической точки зрения инструмент, который создаёт устойчивую и сбалансированную среду для питания растений. Вместо борьбы с последствиями, он работает на опережение: стабилизирует pH, защищает микроэлементы и упрощает уход за раствором даже в сложных условиях.
Его эффективность основана не на «магии» и не на силе реагентов, а на точном расчёте: буферные системы с заданным pKa, способность к хелатированию, стабильность компонентов. Всё это делает pH Perfect незаменимым решением для тех, кто хочет получать прогнозируемый результат — будь то в домашних условиях, в теплице или в промышленной гидропонике.
Если вы стремитесь к стабильности и уверенности в питании своих растений — pH Perfect даст вам эту опору. Просто добавьте его, и вода начнёт работать на вас.
Его эффективность основана не на «магии» и не на силе реагентов, а на точном расчёте: буферные системы с заданным pKa, способность к хелатированию, стабильность компонентов. Всё это делает pH Perfect незаменимым решением для тех, кто хочет получать прогнозируемый результат — будь то в домашних условиях, в теплице или в промышленной гидропонике.
Если вы стремитесь к стабильности и уверенности в питании своих растений — pH Perfect даст вам эту опору. Просто добавьте его, и вода начнёт работать на вас.
Ещё больше интересной информации, акций, бонусов и активностей в нашем тг-канале Simplex Family — подпишитесь, чтобы быть в курсе. А за помощью в подборе удобрений и с прочими практическими вопросами обращайтесь к нашим консультантам.